Predmet kemije. Snovi in njihove fizikalne lastnosti. Predstavitev na temo "Predmet kemija. Snovi" Naravoslovje
diapozitiv 2
Naloga: Dopolni tabele. V prvi tabeli povežite pet pojmov fizičnih teles z enim pojmom snovi, v drugi tabeli pa obratno.
diapozitiv 3
diapozitiv 4
Naloga: Pokaži zmagovalno pot, ki jo sestavljajo imena:
2) snovi
diapozitiv 5
Vprašanja: 1. Kateri delci so prikazani na slikah? 2. Koliko delcev je prikazanih? 3. Preštejte število kemičnih elementov. 4. Katera od slik prikazuje enostavne snovi? Koliko? 5. Kje so upodobljene kompleksne snovi? Koliko?
diapozitiv 6
Naloga: razporedite izraze, ko se velikost delcev poveča:
molekula elektron atomsko jedro
Diapozitiv 7
Naloga: Premaknite risbe, ki prikazujejo atome in molekule, na ustrezne pojme
Kemični element Prosti atomi Kompleksne snovi Enostavne snovi
Diapozitiv 8
Preproste snovi
Žveplo Brom Lastnosti snovi Fosfor Baker Živo srebro Natrij
Diapozitiv 9
Kompleksne snovi
Kremen Lastnosti snovi Namizna sol Cinkova mešanica Voda Rjavi plin
Diapozitiv 10
Lastnosti snovi
Dobite pet centov! Poiščite lastnosti bakra! Naloga toplotno prevodna Rdeče-rjava kovinski sijaj tekoči plin svetloba električno prevodna gladka trda mehka stabilna tempa plastika Odgovor
diapozitiv 11
In zberite funt soli! Pojdite po stopnicah, poiščite lastnosti soli! Naloga Vodotopna ognjevzdržna steklena leska tekoča plinasta prosto tekoča trdna okusna bela mehka upogljiva viskozna Odgovor
diapozitiv 12
Domača naloga
§1,2, vpisi v zvezek. 3,4 Z listom kartona in majhnimi prozornimi vrečkami sestavite zbirko preprostih ali zapletenih snovi, ki se uporabljajo v vsakdanjem življenju.
diapozitiv 13
Seznam uporabljene literature.
O.S. Gabrielyan priročnik za učitelja kemije. 8. razred. M. "Blik plus", 2000 O.S. Gabrielyan Kemija - 8, M. Bustard, 2007 O.S. Gabrielyan, T.V. Smirnova. V 8. razredu študiramo kemijo. M. "Blik plus", 1997 CD Elektronske lekcije in testi "Snovi in njihove transformacije"
Diapozitiv 14
Povezave do uporabljenih slik
Slika bakra http://upload.wikimedia.org/wikipedia/commons/d/dc/Copper_crystals.jpg Slika kremena http://upload.wikimedia.org/wikipedia/commons/c/ce/Quartz_Brésil.jpg Slika žveplohttp:/ /upload.wikimedia.org/wikipedia/commons/4/44/Sulphur-sample.jpg Slika fosforja http://upload.wikimedia.org/wikipedia/commons/8/88/PhosphComby.jpg Slika živega srebra http://upload.wikimedia.org/wikipedia/commons/9/99/Pouring_liquid_mercury_bionerd.jpg Slika broma http://upload.wikimedia.org/wikipedia/commons/b/bd/Brom_amp.jpg Slika rjavega plina http://upload.wikimedia.org/wikipedia/commons/b/bd/Brom_amp.jpg ://upload.wikimedia.org/wikipedia /commons/3/31/Diossido_di_azoto.jpg Slika natrijevega klorida http://upload.wikimedia.org/wikipedia/commons/e/ea/Halit-Kristalle.jpg Slika cinka mešanica http://upload.wikimedia.org/wikipedia/commons /2/2f/Sphalerite4.jpg Slika vode http://upload.wikimedia.org/wikipedia/commons/f/fd/Splash_2_color.jpg
Oglejte si vse diapozitive









Idealna naloga 1. stopnja. Primerjaj fizikalne lastnosti: a) živega srebra in aluminija; b) baker in cink; c) kreda in premog. 2. stopnja. Po katerih dveh najbolj značilnih znakih je dovolj nasprotovati dvema snovmama: a) živemu srebru in aluminiju; b) baker in cink; c) kreda in premog. 3. stopnja. Katere so najbolj znane uporabe naslednjih snovi: a) steklo, b) aluminij? Prisotnost katerih lastnosti se lahko šteje za slabost pri tej njihovi praktični uporabi?


Kemija je čudežna znanost! Na katerem koli področju iztegne roke! Kemija v oblačilih, hrani in vodi, V domu, v zraku, povsod! Barva tekočine se bo hitro spremenila, Ogenj se bo razširil brez tekme, Naravni izdelek bo nadomestil Oseba mora poznati svoje navade! Kmetijstvo, medicina, vesolje... Povsod je povpraševanje po kemiji. Učili ga bomo od zdaj naprej in do stoletja, Konec koncev je kemija tudi človeško telo. Imenujte jo služkinja ali kraljica, Ne gre za ime, Vse naše življenje je znanje kemije. izhod

V pomoč učitelju Diapozitiv 2. Učitelj začne učno uro z uvodnim pogovorom, pri čemer poudarja, da si trenutno ni mogoče predstavljati življenja brez kemije in kemične industrije. Sodobna kemija je prodrla na vsa področja nacionalnega gospodarstva. »Kemija v človeških zadevah na široko razprostira roke. Kamor koli pogledamo, kamor koli se ozremo nazaj - povsod se uspehi njegove uporabe obrnejo pred našimi očmi, «M.M. Lomonosov leta 1751. Nato se razglasi tema lekcije in njeni cilji. Diapozitiv 3. Refleksija. Učitelj prosi učence, da ocenijo svojo pripravljenost za sprejemanje novih informacij. 4. diapozitiv. Učitelj postavlja vprašanja: - Kaj imenujemo telesa? Kakšne lastnosti imajo telesa? - Kaj je snov? Nato razjasni te pojme. Uvaja jasno razliko med pojmi "snov", "telo". Prikazuje vzorce granita, kar kaže, da je telo lahko sestavljeno iz več snovi. 5. diapozitiv. Učitelj povabi učence, da opravijo nalogo: razporedijo imena teles in snovi v stolpce. Nato opravi samopreizkus. 6. diapozitiv. Učitelj postavi vprašanje: - Kakšne lastnosti imajo snovi? Nato učitelj organizira delo po shemi "Najpomembnejše fizikalne lastnosti snovi"

Diapozitiv 7. Učitelj povabi učence, da izberejo lastnost, po kateri se lahko predlagane snovi razporedijo. Učenci opazijo ta znak in razdelijo snovi glede na njihovo agregacijsko stanje. Navzkrižno preverjanje poteka. Diapozitiv 8. Izvaja se korekcija vida. 9. diapozitiv. Ob opazovanju pestrosti znanih in na novo pridobljenih snovi učitelj razloži razliko in podobnost snovi v lastnostih. Učence opozarja na dejstvo, da je možno primerjati snovi, če so poudarjene glavne značilnosti primerjave. Nato učitelj organizira delo pri izpolnjevanju tabele "Primerjava lastnosti snovi." Naredijo sklep o prvi nalogi kemije. Diapozitiv 10. Po pogovoru o primerih transformacij snovi učenci skupaj z učiteljem sklepajo o drugem problemu kemije in definirajo kemijo kot znanost. Diapozitiv 11. Učitelj ponudi učencem, da opravijo eno od nalog po lastni izbiri: 1. stopnja (najnižja). Primerjaj fizikalne lastnosti: a) živega srebra in aluminija, b) bakra in cinka, c) krede in premoga. 2. stopnja (srednja). Po katerih dveh najbolj značilnih znakih je dovolj primerjati dve snovi (glej prvo vprašanje)? 3. stopnja (najvišja). Katere lastnosti so povezane z znano uporabo naslednjih snovi: a) steklo, b) aluminij. Prisotnost katerih lastnosti se lahko šteje za slabost pri tej njihovi praktični uporabi? Diapozitiv 12.13. učitelj pokaže vlogo kemije v znanstvenem in tehnološkem napredku. Bere pesem, ki jo spremljajo barvne ilustracije. Obravnava okoljska vprašanja.


1. stopnja - mitološko razmišljanje
Faza 2 - oblikovanje znanstvenega znanja (starogrška naravna filozofija)
Heraklit: "Svet je eden od vsega, ni ustvaril nobeden od bogov in nihče od ljudi, je večni ogenj, ki se naravno vname in naravno bledi."

Empedokle (490-430 pr.n.št.) - 4 elementi (ogenj, voda, zrak, zemlja) in 2 sili (ljubezen in sovraštvo).
Aristotel (384-322 pr.n.št.) - začela se je enotnost nasprotij: suhost in vlaga, toplota in mraz. V kombinaciji med seboj ta načela tvorijo 4 elemente Empedokla.

Francis Bacon (1561-1626) angleški filozof. Glavna metoda študija kemije naj bo EKSPERIMENT.

Antoine Lavoisier proti koncu 18. stoletja. Dokončal t.i. "kemična revolucija". Od takrat se kemija šteje za znanost o pridobivanju in lastnostih preprostih in zapletenih snovi.

Katera vrstica vsebuje samo snovi?
sol, sladkor, sveča
Voda, železo, žveplo
Baker, žebelj, kisik
Opeka, soda bikarbona, keramično steklo

1) Namizna sol, sladkor, sveča
2) Voda, železo, žveplo
3) Baker, žebelj, kisik
4) Opeka, bakren kovanec, keramično steklo
Zapišite imena snovi s seznama: žebelj, steklo, grafit, ravnilo, aluminij, železo, lijak, škrob, ocetna kislina, glukoza.

Agregacijsko stanje
Gostota
Topnost
Tališče in vrelišče
Električna prevodnost


Moto lekcije:
"Kemija široko raztegne roke v zadevah moških"
M.V. Lomonosov
www.pmedia.ru

Namen lekcije:
srečati se
- - predmet kemija;
- - enostavne in zapletene snovi;
- -lastnosti snovi;
- - oblike obstoja kemičnega elementa.

naravne znanosti
1 . Katere znanosti preučujejo naravo?
2. Kaj preučuje biologija; fizika; geografija; astronomija; geologija?
3. Zakaj ste v 7. razredu začeli študirati fiziko, v 8. pa kemijo?



Kaj preučuje kemija?
ŠTUDIJ KEMIJE
SNOVI
"Oče kemije" Robert Boyle (1627 - 1691)
LASTNOSTI SNOVI
TRANSFORMACIJE SNOVI

Kemija - znanost o snoveh lastnosti in transformacije.
Telo
Snov
molekule
atomi

Snov – iz česar so sestavljena fizična telesa Kemični element je določena vrsta atoma
Snovi
Snovi
Preprosto
(vodik,
kisik)
Kompleksno
(voda, sladkor)
Naravni
(karbonska
plin)
Sintetika
cal
(polietilen)

Razmislite o molekularnih modelih. Kakšne so podobnosti in razlike med njimi? Katera od snovi je preprosta in katera zapletena? zakaj?
- Snovi
vodik
Voda
Kisik

Oblike obstoja kemični elementi
preprosta snov
kompleksna snov



Snovi, ki jih tvorijo atomi enega kemičnega elementa, se imenujejo preprosta


Snovi, ki jih tvorijo atomi različnih kemičnih elementov, se imenujejo zapleteno

Lastnosti snovi
fizično
kemični
- agregatno stanje
- vonj
- topnost v vodi
- toplotna prevodnost
- električna prevodnost
- gostota
- sposobnost reagiranja z drugimi snovmi


Tekoče snovi
Žveplova kislina
Rastlinsko olje

Plinaste snovi
Kisik
Ogljikov dioksid

Vaja #1
Ugotovite, katera od predlaganih snovi je preprosta in katera zapletena.




Lastnosti
Sestavljen
Kemija
Aplikacija
Lastnosti snovi so znaki, po katerih se snovi med seboj razlikujejo ali so si med seboj podobne.

Vaja #2
- Navedite, kje se o kisiku govori kot o kemičnem elementu in kje - kot o preprosti snovi:
- A) kisik je rahlo topen v vodi;
- B) molekule vode so sestavljene iz dveh atomov vodika in enega atoma kisika;
- C) zrak vsebuje 21 % kisika (volumensko);
- D) Kisik je del ogljikovega dioksida.

Načrt za opis fizikalnih lastnosti snovi
1. V kakšnem agregacijskem stanju – plinastem, tekočem ali trdnem – je snov v teh pogojih?
2. Kakšne barve je snov? Ali ima sijaj?
3. Ali ima snov neprijeten vonj?
4. Ali snov kaže plastičnost, krhkost, elastičnost?
5. Ali se snov raztopi v vodi?
6. Kakšno je tališče in vrelišče snovi? (Glej referenčne knjige.)
7. Kakšna je gostota snovi? (Glej referenčne knjige.)
8. Ali ima snov toplotno in električno prevodnost? (Glej referenčne knjige.)

Vaja #3
Opišite fizikalne lastnosti ocetne kisline, sladkorja, soli, bakra, aluminija po predlaganem načrtu.
(Učbenik S.10)

Pokaži ujemanje med imeni snovi in njihovimi lastnostmi.
- železo
- Kisik
- aluminij
- klorofil
- Sladkor
- Briljantno
- Brezbarvna
- Pregleden
- Svetloba
- rdeča opeka
- sladko
- Zelena

Izberite pravo besedo
A) Steklo - bučka
Jeklo - (ruda, lito železo, žlica)
B) Aluminij - trden
Živo srebro - (svetleč, srebrno bel, tekoč)
C) Kisik - brez vonja
Amoniak - (lažji od zraka, brezbarven, ima oster vonj)
D) Baterija - lito železo
Vaza - (voda, steklo, snov)

Kemija in varstvo okolja

Domača naloga
2. odstavek
RT s. 4 - 5 (v celoti),
Z. 8 - 9 # 10-13
Cilji lekcije:
- izobraževalni: oblikovati razumevanje predmeta kemija. Podati začetne pojme snovi, kemičnega elementa, o preprostih in zapletenih snoveh, o treh oblikah obstoja kemičnega elementa.
- Izobraževalni: razvoj logičnega in pomenskega mišljenja učencev, spomina, kemičnega jezika, pa tudi sposobnosti izvajanja samostojnih dejavnosti v razredu.
- negovanje: gojiti kulturo umskega dela, razvijati komunikacijske lastnosti posameznika.
Vrsta lekcije: učenje nove teme.
Metoda poučevanja: delno iskalno, raziskovalno, problematično.
Organizacijske oblike: pogovor, samostojno delo, praktično delo.
Materialna podpora pouku: Računalnik, projektor, platno.
Na razstavni mizi: zbirka izdelkov iz stekla in aluminija. Železni opilki, žveplo, magnet, list belega papirja in kozarec vode.
Na študentskih mizah: sladkor, rastlinsko olje, pesek, aluminij - v epruvetah in voda v bučki, slepci za načrtovanje laboratorijskega poskusa.
Motivacija: Posodobitev znanja.
Začnemo z vprašanjem "Kaj veš o kemiji?"
Med pogovorom pogovor pripeljemo do glavnega toka pomena kemije,
z uporabo stojala" Kemija v našem življenju”.
Kemija ima ogromen potencial, ustvarja prej neznane materiale,
Olajša delo osebe, oblačil, prihrani čas, ustvarja udobje in udobje ter celo spremeni videz ljudi.
Toda ista kemija lahko postane nevarna za zdravje, celo smrtonosna ...
Pisec znanstvene fantastike in biokemik Isaac Asimov je zapisal: "Kemija je smrt, zapakirana v kozarce in škatle ..."
Kar je bilo povedano, včasih drži ne le v zvezi s kemijo, ampak tudi v zvezi z elektriko, gospodinjskimi aparati in prometom.
Brez elektrike ne moremo živeti, a gola žica je smrtonosna, vsi radi gledamo televizijo, a za njeno zadnjo ploščo je napetost na tisoče voltov, potrebujemo avto, a ljudje pogosto umirajo pod njegovimi kolesi.
Podobno tudi uporaba dosežkov sodobne kemije od ljudi zahteva visoko splošno kulturo, veliko odgovornost in seveda znanje.
Nato študente pripeljemo do ideje, da sodobni človek ne more brez tega, kar mu daje kemija, in da ne bi postal kot otrok, ki se igra z ognjem in ne razume, s čim se igra, mora imeti sodoben človek vsaj splošno predstavo o predmetu kemije. Naša današnja naloga je ugotoviti, kako je nastala ta starodavna znanost in kaj je predmet preučevanja te znanosti?
Študij novega materiala in primarna kontrola:
Demonstracija predstavitve v programu PowerPoint »Zgodovina kemije« (Priloga 1) *.


Kaj preučuje kemijska znanost? Kemija se uči: (piše na tablo in v zvezek):
- Snovi.
- Lastnosti snovi.
- Transformacije snovi.
Demonstracija zbirke izdelkov iz stekla in ločeno aluminija.
- vprašanje: kaj imajo vsi ti predmeti skupnega (prikazane so epruvete, bučke, kozarec). Odgovor: izdelani so iz stekla;
- vprašanje: zakaj enake epruvete ni mogoče izdelati iz aluminija? Kakšna je razlika med steklom in aluminijem? Odgovor je lastnosti;
demonstracija: delovanje magneta na železne opilke in žveplo,
v kozarec vode dajte železne opilke in žveplo.
Frontalna razprava o lastnostih železnih opilkov in žvepla.
Sidranje: izvedemo laboratorijski poskus in izpolnimo rezultat v predlaganih praznih obrazcih po modelu:
Vzorec :
Laboratorijske izkušnje.
Tema: Preučevanje fizikalnih lastnosti različnih snovi.
Cilj:________________________________
Rezultat dela.
1. Vsebini vsake od štirih epruvet dodajte nekaj vode.
2. Opiši, kaj se dogaja v epruveti.
3. Od snovi, katerih lastnosti ste pravkar opisali, navedite tiste, ki:
a) so v enakem agregatnem stanju;
b) praktično netopen v vodi.
4. Primerjaj lastnosti sladkorja in peska, navedi podobnosti in razlike v lastnostih teh snovi.
ZAKLJUČEK: Različne snovi imajo lahko tako _____________ kot
In ________________ lastnosti.
Vprašanje razredu: Kaj je fizično telo? Navedite primere?
Zaključki: (vnos v zvezek)
- Materija je tisto, iz česar so sestavljena fizična telesa.
- Kemija je znanost o snoveh, njihovih lastnostih in transformacijah.
Vprašanje: zakaj morate poznati lastnosti določenih snovi? Odgovor je, da jih uporabite v svojo korist.
Zaključek tega pogovora je povzet takole: 
Spomnimo se, kaj vemo iz fizike:
Snovi so sestavljene iz molekul in molekule so sestavljene iz
drobnih atomov, ki pa
razlikujejo se kot znamke avtomobilov: Volga, Muscovite,
Žiguli itd. Skupno je približno 118 takšnih vrst atomov.
Torej vpis v zvezek:
Določena vrsta atoma se imenuje kemični element.
Pojasnimo, da ima vsak kemični element
tri oblike obstoja. (prenesite diagram s plošče v zvezke) 
Na primer:
Hitro pritrditev:
1.
Predlaga se, da učenci poslušajo izjavo in dvignejo desno roko, če gre za preprosto snov, in levo roko, če gre za element:
-dušik ne podpira izgorevanja;
- železo ima sposobnost magnetiziranja;
- vsebnost kisika v žveplovem(IV) oksidu je manjša kot v žveplovem(VI) oksidu;
- molekula amoniaka je sestavljena iz dušika in vodika;
- rumeno žveplo;
- železo je del številnih multivitaminov.
2.
Dopolni diagram: 
Nadzor asimilacije:
Preizkusite samokontrolo s samotestiranjem – odgovori so pripravljeni vnaprej. (Dodatek 2).
Asimilacijo ocenjujemo po številu pravilnih odgovorov.
1.
Vsak predmet, ki nas obdaja, je:
a) fizično telo
b) snov
2.
Steklena vaza, steklena skodelica, steklena bučka je:
a) telesa
b) snovi.
3.
Snov je:
a) iz česa je sestavljeno fizično telo;
b) kateri koli predmet okoli nas.
4.
Kateri od naslednjih stavkov se nanaša na steklo kot fizično telo?
a) razbil je okensko steklo;
b) vaza je steklena.
5.
Lastnosti snovi so:
a) značilnosti, po katerih so si snovi podobne ali drugačne;
b) barvo snovi.
6.
Zapišite, katere kakovostne pridevnike - krhek, kratek, zrcalni, smrdljiv, drobljiv, simetričen, porozen, ukrivljen, srebrn, taljiv - je mogoče pripisati:
a) za snovi;
b) telesom;
c) tako za telesa kot za snovi.
7.
Izberite preprosto snov:
a) kisik
b) voda
c) žveplova kislina
d) aluminijev oksid
8.
Izberite mešanico snovi:
a) zrak
b) magnezijev oksid
c) aluminij
d) železov sulfid.
Razmislek in povzetek:
Na koncu še povejte svoje vtise o lekciji. Če želite to narediti, dopolnite stavke, posvečene današnjemu času.
Danes sem izvedel
Bil sem presenečen
Rad bi _______________________________________________
Domača naloga:
Ko otrokom povedo domačo nalogo, naj razložijo vrstni red njenega izvajanja. Katere vaje je mogoče izvajati ustno, katere pa pisno §1., pr. 1 (ustno).
Literatura:
- Gabrielyan O.S. Učbenik kemije 8. razreda za izobraževalne ustanove Moskva "Business Bustard", 2006
- Gabrielyan O.S., Voskoboynikova N.P., Yashukova A.V. Priročnik za učitelja, 8. razred Moskva "Businessbust", 2002
- Gorkovenko M.Yu. "Čiste lekcije razvoja lekcije 8 razred" Moskva "Vako", 2005
- Bocharova S.V. "Kemija 8. Načrti lekcije "Volgograd. "Učitelj - Ast", 2004
Internetni viri:
- Alchemist.ru - Kunstkamera
- http://a-ivan.by.ru
- http://ru.wikipedia.org/wiki/History_of_chemistry
- http://www.physchem.chimfak.rsu.ru/Source/History/Sketch_2.html
 Snovi in njihove fizikalne lastnosti
Snovi in njihove fizikalne lastnosti Razvrstitev, zgradba, prehrana in vloga bakterij v naravi
Razvrstitev, zgradba, prehrana in vloga bakterij v naravi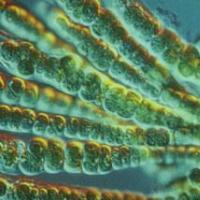 Bakterije - najstarejši organizmi na Zemlji Bakterije - najstarejša skupina živih organizmov
Bakterije - najstarejši organizmi na Zemlji Bakterije - najstarejša skupina živih organizmov Epiteti, metafore, personifikacije, primerjave: definicije, primeri
Epiteti, metafore, personifikacije, primerjave: definicije, primeri Bronhialna astma Bronhialna astma
Bronhialna astma Bronhialna astma Stara zgodovina Rimskega cesarstva
Stara zgodovina Rimskega cesarstva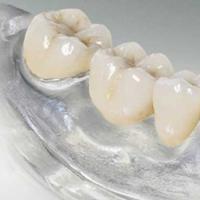 Fleksibilne odstranljive proteze: zasnova, značilnosti in prednosti Različne mehke proteze s fotografijami
Fleksibilne odstranljive proteze: zasnova, značilnosti in prednosti Različne mehke proteze s fotografijami